
GLP:良好实验室管理规范(Good Laboratory Practice),GLP研究包括但不限于不同FDA中心收到的临床毒理学、安全药理学研究和医疗器械安全研究。
翻译GLP研究报告的目的在于确保将非英语原文转换成英语后的报告,在向 FDA 提交时能够清晰、准确、完整且真实地呈现。
FDA近期发布的行业指南《GLP研究报告的翻译:问答(Translation of GLP Study Reports: Questions and Answers)》有两个关键点:
翻译人员应当具备相应的教育、培训和经验,熟悉医学和科学文档的翻译工作。
翻译后的GLP研究报告应清晰、准确、完整、真实地表示原始报告文本和带标题的表格,包括但不限于研究摘要、材料和方法、结果、讨论和结论部分,并应使用与原始报告相同的格式、表格、附录和修订。
雅瑞思医学翻译团队有上百名药学、医学、物理学、制造学、工程学专职翻译专家。笔译团队均由持有翻译资格证且从事翻译工作十年以上的资深翻译和审校组成。
同时,雅瑞思一直致力于医学翻译人才的储备,译员开发途径包括智联、boss直聘、51找翻译、各类译员QQ群、领英、Proz、upwork、freelancer、facebook等。对于译员的筛选,我们会从所学专业、学历证书、从业年限等多个维度考量,配合规范完备的筛选流程以确保译员达到我司医学翻译的标准。
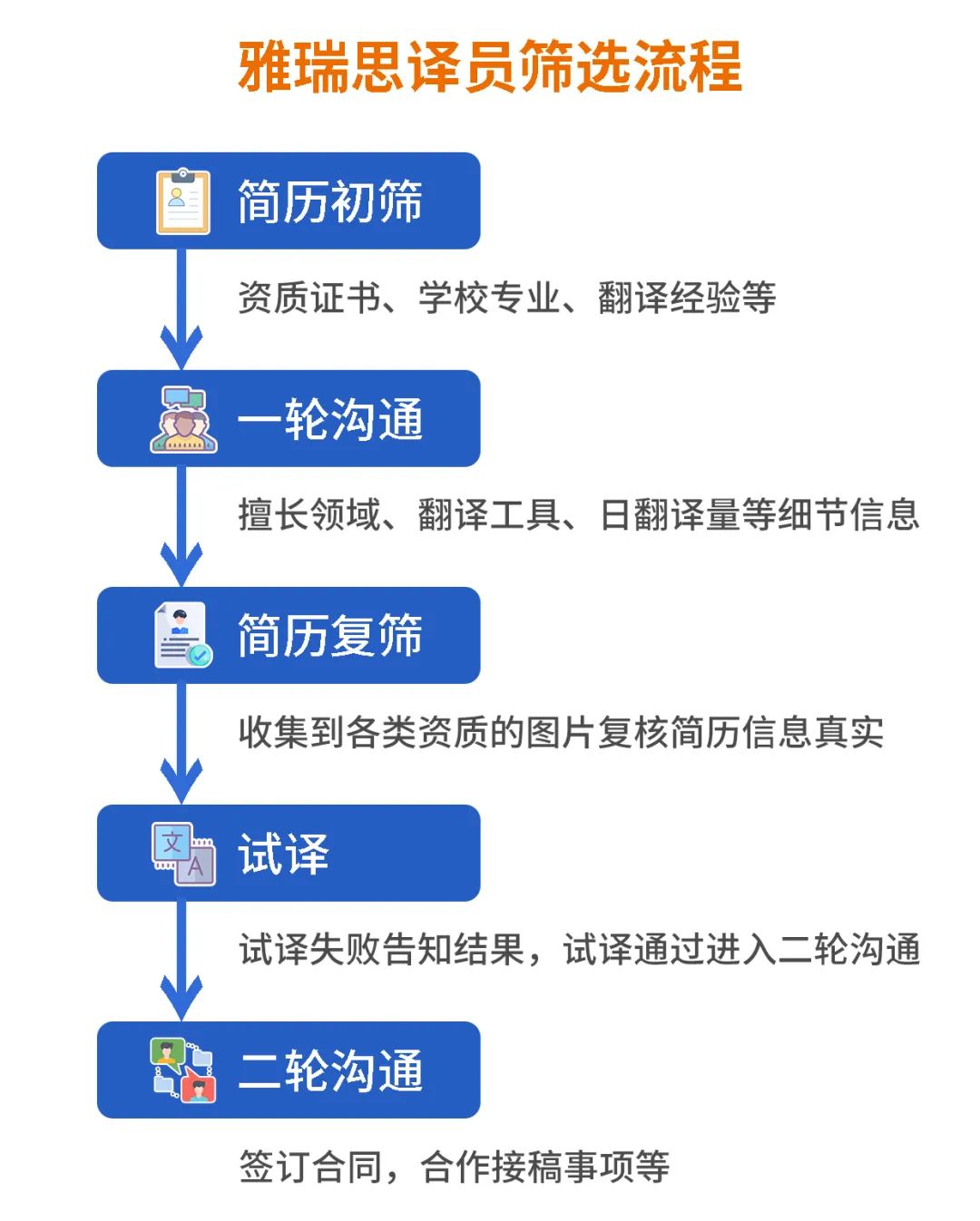
雅瑞思为翻译过程制定了标准操作程序(SOP),包括对与翻译活动相关的文档的要求,例如翻译声明、翻译准确性验证和完整性检查等,以确保提交给FDA的翻译非临床数据是可靠的。


雅瑞思医学翻译严格遵守管理流程和翻译声明的内容规范,制定了标准化的GLP研究报告翻译流程和操作规程,明确了翻译人员资质要求、翻译过程文档化管理、翻译正确性核查流程、翻译版本完整性检查等,既满足客户个性化需求,也满足监管机构对翻译质量的要求。